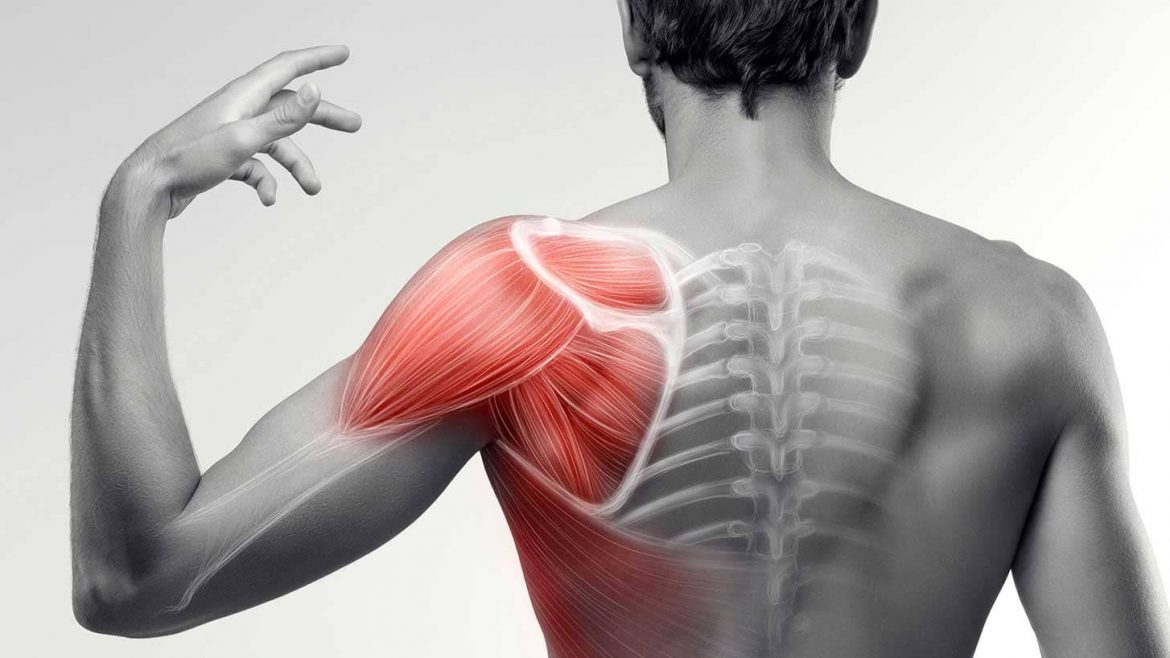
La hiperextensión de rodilla es un fenómeno habitual durante la marcha en personas que han sufrido DCA.
Esta extensión de la rodilla durante la fase de apoyo de la marcha que va mas allá de la posición fisiológica supone un mecanismo adaptativo para conseguir estabilidad cuando no se puede conseguir de otra manera.
La preocupación de los terapeutas viene de que a medida que se hacen hiperextensiones repetidas, que muchas veces son bruscas, se desarrolla una hiperlaxitud de las estructuras posteriores de la rodilla, pudiendo llegar a provocar deformidad y dolor a largo plazo.
Inicialmente, el bloqueo de rodilla es una estrategia que aporta la estabilidad suficiente para conseguir adelantar el siguiente pie, sin embargo, también supone una limitación en las estrategias de equilibrio de la persona. Es decir, aportan mucha estabilidad en una posición concreta al fijar la articulación, pero fuera de esa posición no aportan nada de estabilidad.
Si realizamos una búsqueda bibliográfica sobre el tema hallamos muy pocos estudios y una gran falta de consenso acerca de las causas y mecanismos subyacentes. Principalmente los estudios que encontramos buscan una relación entre fuerza en cuádriceps, isquiotibiales y gastrocnemios con la hiperextensión de rodilla durante la marcha.
Entre estos estudios nos llama la atención el siguiente:
«The relationship of lower limb muscle strength and knee joint hyperextension during the stance phase of gait in hemiparetic stroke patients»;
Lo que encontraron fue una relación entre la debilidad de flexores plantares y la hiperextensión de rodilla durante la fase de apoyo medio. No se consiguió ningún otro resultado estadísticamente significativo, aunque la debilidad de flexores dorsales de tobillo estuvo cerca de alcanzar una asociación significativa.
Desgraciadamente el pequeño número de participantes en el estudio no permitió obtener mejores resultados, pero aun así nos hace reflexionar sobre la importancia de la musculatura de la pierna para la estabilización de la rodilla. Después de todo, los flexores plantares y dorsales son los encargados de estabilizar la tibia en la posición necesaria en la fase de apoyo de la marcha, si estos no tienen suficiente fuerza para realizarlo, ¿cómo van a mantenerse estables los segmentos superiores?
También es llamativo como no encuentran relación entre extensiones de rodilla y la hipertensión, cuando es muy habitual relacionarlos en la rehabilitación.
Fuerza muscular, rango articular, restricciones neurales o fasciales, alteraciones sensitivas, postura corporal… son muchas las piezas que forman el puzzle de este fenómeno, y este estudio nos aporta un poco más de información acerca de una de ellas. En el trabajo en clínica, un análisis y abordaje global son necesarios para obtener los mayores resultados.
Aquí está disponible el articulo completo en inglés:
https://
Por otro lado, es más que interesante el análisis que realiza Javier Sánchez en su canal Hemispherics sobre la evidencia del bloqueo de rodilla durante la marcha tras un ictus: