Pues tenemos bastantes argumentos para desmentir dicha afirmación, coomo por ejemplo el siguiente estudio:
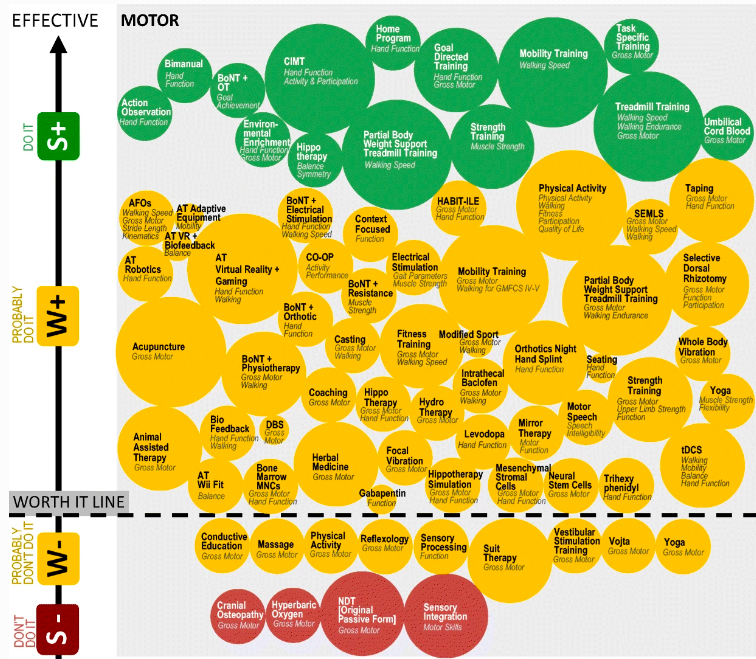
En este estudio se realizó un trabajo de entrenamiento de la fuerza de extremidades inferiores con dos grupos diferenciados, formados por 10 sujetos cada uno. El primer grupo trabajó solo la extremidad más afecta (aumentando la carga de ésta), mientras que el otro trabajó ejercicios que incluían ambas extremidades inferiores. Los resultados fueron supuestamente sorprendentes, ambos grupos recuperaron tanto la fuerza, como el equilibrio y la capacidad de la marcha. Sin embargo, el grupo que incluyó un trabajo de ambas extremidades inferiores (el segundo) obtuvo mejores resultados a su vez, que el que trabajó tan solo una.
Es por ello que la necesidad de objetivar la fuerza muscular en nuestros pacientes neurológicos tiene especial necesidad e interés, y nosotros lo hacemos desde el dispositivo Kforce Muscle Controller, quien a través de sus sensores de presión, se obtiene un valor de la fuerza de la acción muscular que te interese valorar, ya sea de las extremidades, cabeza o tronco, obteniendo un resultado más objetivo en la variable fuerza.
A partir del análisis de dicho movimiento aislado, por ejemplo, fuerza de cuádriceps en sedestación, podemos obtener el resultado de la capacidad de contracción del músculo, y establecer una correlación con la cantidad de fuerza que se necesita para realizar una función o actividad de la vida diaria en la que sea necesaria un movimiento de extensión de rodilla tanto en concéntrico como en excéntrico. Por tanto, y siempre utilizando el razonamiento clínico, podemos encontrar relevante una implicación de la debilidad siendo ésta determinate en las capacidades básicas para el desarrollo de la actividad o función.
Por tanto, el registro objetivo de la fuerza nos puede ser de gran ayuda, y si además lo trabajamos de manera específica tal y como se muestra en el estudio anteriormente citado, podemos optimizar los resultados funcionales en nuestros pacientes. Así pues, el trabajo de ambas extremidades inferiores es más enriquecedor que el de una sola, ya tenemos un motivo más para desterrar aquello de «pierna mala y pierna sana». Vamos a llamarlas, pierna izquierda y pierna derecha.
Para descargar el estudio: https://
Para más información sobre el dispositivo: fisioterapia@neurofuncion.com